Черви попробовали таблетку долголетия. Последние достижения генной терапии вызывают шок
Потенциал генной терапии – огромен: манипуляции с генами уже позволили продлить жизнь ряда живых организмов в несколько раз. «Таблетки долголетия», которые можно «съесть и запить водой», уже найденные для червяков, — на гране фантастики, если речь идет о продлении жизни человека. Сегодня ведется активный поиск препаратов генной терапии и способов их доставки в клетки человека. Последние достижения генной терапии вызывают шок.
Человек и круглый червь Caenorhabditis elegans — организмы похожие. Около половины генов червяка можно найти и у человека. В Библии есть выражение «Аз есмь червь…» (Псалтирь 21:7), которое хорошо иллюстрирует такое сходство и согласуется с эволюционными представлениями о родстве этих видов. Это имеет важное практическое значение — многие генетические болезни человека есть и у червяка, а изучать червяка удобней, чем человека.
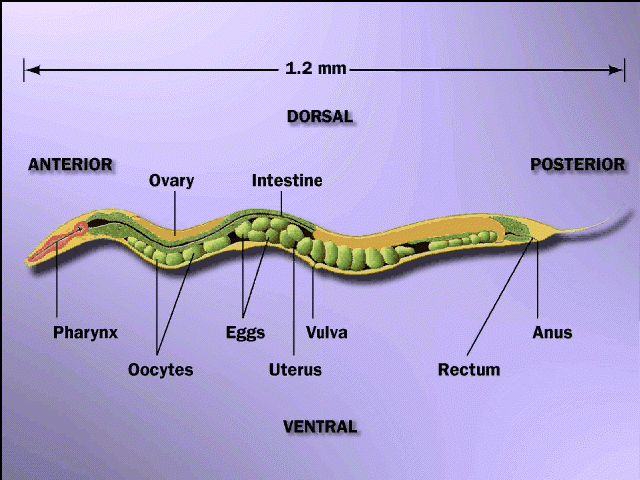
На червяке сделано множество открытий, например, найдены гены, отключив которые можно продлить жизнь этого организма в 2,5—10 раз. Избирательно отключать гены червяка можно, добавляя им в пищу специальные молекулы двухцепочечной РНК (РНК — промежуточные молекулы, передающие информацию от генов для синтеза белков). То есть для червяка найдена «таблетка долголетия».
Два ключевых элемента в работе такой терапии — специальные каналы, по которым двухцепочечная РНК разносится по всему организму, и сложная система РНК-интерференции, механизма, который направленно подавляет производство белка, кодируемого геном-мишенью. У человека тоже есть РНК-интерференция, и есть каналы, похожие на каналы червяка, но такая удобная система доставки информационных молекул по всему организму пока не обнаружена. В генной терапии человека используют другие системы доставки, например вирусы.
Ретровирусы умеют создавать ДНК-копии своего генома и встраивать их в хромосомы клеток хозяина. Наиболее известными примерами ретровирусов являются вирус иммунодефицита человека (ВИЧ) и вирус гепатита Б (для терапии используются другие). С помощью генной инженерии можно удалить часть генома ретровируса, которая вызывает заболевание, и вставить полезный ген. Если в клетке какой-то ген испорчен, а вирус принесет исправную копию этого, можно ожидать восстановление утраченной функции, выздоровление клетки.
Лечение наследственного иммунодефицита
В иммунитете человека важную роль играют клетки — лимфоциты. При нормальном развитии иммунной системы предшественники лимфоцитов претерпевают генетические перестройки, из-за которых возникает множество популяций лимфоцитов, каждая с уникальным набором рецепторов — белков, необходимых для узнавания чужеродных агентов.
Поскольку разнообразие рецепторов оказывается огромным, практически на любую инфекцию найдется группа лимфоцитов, способных ее распознать. При проникновении инфекции в организм распознавшие ее лимфоциты начинают активно делиться. Важную роль при этом играют вещества интерлейкины и рецепторы к ним. Если рецептора к интерлейкинам нет или он испорчен, иммунные клетки практически не размножаются, возникает синдром тяжелого комбинированного иммунодефицита.
В 1972 году в Техасе родился мальчик Дэйвид Веттер, которому поставили такой диагноз. Мальчик стал известен тем, что 12 лет прожил в стерильном помещении, в «пузыре». Несмотря на меры предосторожности, мальчик погиб в результате тяжелой инфекции вирусом Эпштейна-Барра. В те времена не было лекарства. Сегодня с помощью генетически модифицированных ретровирусов можно внедрить правильную копию гена рецептора интерлейкинов в лимфоциты и исправить дефект. Таким образом вылечены уже десятки детей.
Лечение рака
Ретровирусы — не единственный тип вирусов, который используется для генной терапии. Аденовирусы (например, возбудители бронхита, конъюнктивита, простуды) не встраивают свой геном в хромосомы хозяина. Это имеет одно преимущество: нет риска того, что вирусная ДНК, встраиваясь в хромосому, случайно повредит какой-нибудь важный ген (такие вставки могут приводить к заболеваниям, например, к раку). Более того, генетически модифицированные аденовирусы показали себя с хорошей стороны в борьбе с раком.
Рак возникает тогда, когда клетка начинает неконтролируемо делиться, как правило, в результате повреждений целого ряда генов. Генетический анализ показал, что очень часто в раковых клетках присутствует мутация в гене, который кодирует белок p53. Если клетка сильно повреждена, белок p53 может препятствовать делению клетки и даже заставить ее совершить «самоубийство». Именно поэтому во многих случаях, чтобы клетка стала раковой, ген белка p53 должен испортиться.
В таких случаях привнесение исправного гена p53 с помощью вируса должно остановить развитие опухоли. Этот подход лежит в основе препарата гендицина, который прошел клинические испытания в Китае. Гендицин содержит генетически измененный аденовирус, который не способен самостоятельно размножаться и вызывать болезни, но содержит работающую копию p53.
Другой способ борьбы против рака — использование иммунной системы. В ряде случаев раковые клетки отличаются от нормальных клеток маркерами (особыми белками в их мембране). Эти маркеры могут узнаваться клетками иммунной системы — лимфоцитами. Если у человека отсутствуют лимфоциты с подходящими рецепторами, иммунная система не распознает раковые клетки и не борется с ними.
В 2006 году в престижном научном журнале Science были опубликованы результаты применения следующей процедуры лечения меланомы (рака кожи). У больного берутся лимфоциты и помещаются в пробирку, а затем модифицируются с помощью ретровирусов: в них вставляется ген рецептора к раковому маркеру, свойственному меланоме. Лимфоциты запускаются обратно в кровь пациента. Применение этой процедуры привело к регрессии метастазирующей меланомы у нескольких пациентов: на клетки меланомы возник иммунный ответ.
У возбудителя псевдотуберкулеза, родственника чумы, есть ген, который позволяет бактерии проникать внутрь клеток человека в составе мембранных пузырьков. У возбудителя листериоза есть ген, отвечающий за разрушения мембранных пузырьков и высвобождение содержимого бактерии внутрь клетки. В безвредную кишечную палочку можно встроить упомянутые два гена, а также ген двухцепочечной РНК, способной отключить производство определенного онкогена (белка, вызывающего рак). Такая бактерия попадает в клетку как чумная палочка, высвобождается как листерия и запускает противораковый механизм. Таким образом, еще одно лекарство от рака, недавно проверенное на клетках человека, основано на использовании наших злейших врагов.
Лечение врожденной слепоты
Амавроз Лебера — наследственное заболевание сетчатки глаза, ведущее к нарушению работы и последующей смерти светочувствительных клеток (палочек и колбочек). Чаще всего это происходит из-за отсутствия работающей формы гена RPE65, без которого нарушается производство зрительного пигмента. Опыты на собаках и грызунах, а также последующие исследования на людях показали, что можно добиться улучшения зрения больных, если внести хорошую копию гена в клетки сетчатки глаза. Для этого ген RPE65 встраивают в аденовирус, а затем производят инъекцию вируса в сетчатку с помощью тонкой иголки.
При особо тяжелых нарушениях зрения колбочки и палочки разрушены полностью. Но кроме палочек и колбочек в глазу находится слой нервных клеток, которые обрабатывают зрительную информацию и посылают ее в мозг. В то время как у человека для распознавания света используется целая группа взаимодействующих белков, у некоторых одноклеточных зеленых водорослей используется один-единственный белок, который является чувствительным к свету ионным каналом, пронизывающим клеточную мембрану.
Если канал осветить, он открывается и впускает в клетку положительные ионы, меняя ее электрический потенциал. Если клетка — нейрон, изменение потенциала на ее мембране приведет к возникновению нервного импульса. Возникла идея, что можно встроить ген светочувствительного канала растений в нейроны глаза, чтобы сделать их чувствительными к свету. На ослепших грызунах было показано, что после инъекции вируса, содержащего ген растительного фоточувствительного канала, в зрительные отделы мозга начинают поступать сигналы от глаз.
Перспективы
Еще один подход заключается не в лечении заболеваний, а в предотвращении их на эмбриональных стадиях развития. Отчасти это уже реализовано при генетической диагностике, сопутствующей искусственному оплодотворению: можно выбрать зародыша, лишенного известных генетических заболеваний. В будущем ученые научатся использовать генную инженерию для улучшения и исправления генов человека. Еще один важный момент заключается в том, что генная терапия заставляет пересмотреть наше отношение ко многим естественным врагам человека. Даже опасные вирусы и бактерии могут превратиться в наших союзников в руках опытного генного инженера.
Александр Панчин, Новая Газета
Tweet










